Descripción
Este test es un inmunoensayo para la detección cualitativa de anticuerpos que incluyen IgG, IgM e IgA frente a las especies que conforman el complejo Leishmania donovani (incluyendo Leishmania infantum, agente causal de la Leishmaniosis canina), en suero o plasma. Esta prueba está destinada a ser utilizada como una prueba de detección y como una ayuda en el diagnóstico de la Leishmaniosis canina. Cualquier muestra positiva con este test debería confirmarse con una prueba alternativa (disponible de forma gratuita en nuestro laboratorio).
La Leishmaniosis, es una infección diseminada por el mosquito Phlebotomus, que adquiere la infección al alimentarse de los animales infectados. Se trata también de una zoonosis que afecta a personas inmunodeprimidas.
Existen numerosas pruebas de laboratorio para el diagnóstico de la Leishmaniosis, como son la identificación del microorganismo en médula ósea, ganglio linfático o bazo, las técnicas de PCR o la detección de anticuerpos por ELISA o IFI. Sin embargo, todas ellas requieren instrumental y personal especializados. La prueba rápida de Leishmania Ac es un prueba serológica basada en proteínas recombinantes, que detecta anticuerpos que incluyen IgG, IgM e IgA frente al complejo L. donovani (incluyendo L. infantum). Esto proporciona un resultado fiable en tan solo 10 minutos sin ningún requisito de instrumentación.
PRINCIPIO
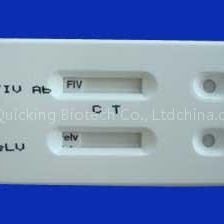
El dispositivo Leishmania Ab Prueba Rápida es un inmunoensayo cromatográfico de flujo lateral. El dispositivo de prueba consiste en:
1) Una almohadilla de conjugado de color burdeos que contiene el antígeno recombinante de L. donovani conjugado con oro coloidal un conjugado de conejo IgG-oro.
2) Una tira de membrana de nitrocelulosa que contiene una banda para el resultado positivo (banda T) y una banda de control (banda C). La banda T está recubierta con un conjugado de antígeno de L. donovani, y la banda C está recubierta con anticuerpo IgG de cabra anti-conejo.
Cuando un volumen adecuado de suero a analizar se dispensa en el pocillo de muestra de la casete de prueba, la muestra migra por acción capilar a través de la casete. Si hay anticuerpos contra L. donovani presentes en la muestra se unirán a los conjugados de Leishmania. El complejo inmunológico es capturado en la membrana por el antígeno que la recubre, formando una banda T color borgoña, que indica que es positivo y por tanto existe un nivel de anticuerpos contra L. donovani por encima del nivel que se considera positivo.
La ausencia de la banda T indica un resultado negativo. La prueba contiene un control interno (banda C) que debe exhibir una banda de color burdeos con independencia del desarrollo del color en la banda T. De lo contrario, el resultado de la prueba no es válido y la muestra debe ser analizada de nuevo con otro dispositivo.
CONTENIDO
Dispositivos individuales para el test.
Pipetas desechables para añadir la muestra.
Tampón.
Prospecto.
PRECAUCIONES
-Solo para uso profesional.
-No utilizar después de la fecha de caducidad indicada en el paquete. No utilice la prueba si su bolsa de aluminio está dañada.
-Este kit contiene productos de origen animal. Aunque el origen de los productos es conocido y está certificado esto no garantiza totalmente la ausencia de agentes patógenos transmisibles. Por lo tanto se recomienda que estos productos sean tratados como potencialmente infecciosos, y manejados siguiendo las precauciones de seguridad habituales (no ingerir o inhalar).
– Evitar la contaminación cruzada de las muestras mediante el uso de un nuevo envase para la recogida de muestras de cada nuevo animal.
– Lea cuidadosamente el procedimiento completo antes de realizar cualquier prueba.
– No comer, beber o fumar en el área donde se manejan las muestras y los estuches. Manejar todas
las muestras como si contuvieran agentes infecciosos. Observe las precauciones establecidas contra
riesgos microbiológicos durante los procedimientos y siga los procedimientos estándar para desechar los residuos.
– Use ropa protectora, como batas de laboratorio, desechables, guantes y protección para los ojos cuando las muestras son analizadas.
– La solución salina tamponada contiene azida sódica que puede reaccionar con el plomo o el cobre y formar potencialmente azidas metálicas explosivas. Cuando se deshaga de la solución salina tamponada o las muestras extraídas, aclare siempre al ras con agua abundante para evitar la formación de ácidos.
– No intercambiar o mezclar reactivos de diferentes lotes.
– La humedad y la temperatura pueden afectar los resultados.
– Los materiales de prueba utilizados deben ser desechados según las normativas vigentes.
INSTRUCCIONES DE ALMACENAMIENTO
Todos los reactivos están listos para usar. Almacenar los dispositivos no utilizados sin abrir entre 2 ° C y 30 ° C. Los sueros o sangres deben atemperarse a temperatura ambiente durante 10 minutos antes de su uso, así como los dispositivos y el tampón si están almacenados en frigorífico. El dispositivo de prueba es estable hasta la fecha de caducidad impresa en la bolsa sellada. No congelar el kit ni exponer el kit de más de 30 ° C.
TOMA DE MUESTRAS Y MANIPULACIÓN
-El dispositivo Leishmania Ab Prueba Rápida se puede realizar utilizando sangre entera, suero o plasma.
– Separe el suero o plasma de la sangre tan pronto como sea posible para evitar la hemólisis. Utilice únicamente muestras no hemolizadas.
– La prueba debe realizarse inmediatamente después de la recogida de muestras. No deje el
muestras a temperatura ambiente por períodos prolongados. Las muestras de suero y plasma pueden ser almacenadas a 2-8 ° C durante un máximo de 3 días. Para el almacenamiento a largo plazo, las muestras deben mantenerse por debajo de -20 ° C (solo suero o plasma).
-La sangre total extraída por punción venosa debe ser almacenado a 2-8 ° C si la prueba se va a ejecutar dentro de los dos días desde su toma. No congelar muestras de sangre total.
-Llevar las muestras a temperatura ambiente antes de la prueba. Las muestras congeladas deben estar completamente descongelada y homogeneizadas antes de la prueba. Las muestras no deben ser congeladas y descongeladas en repetidas ocasiones.
– Si las muestras deben ser trasportadas, deben ser empaquetadas cumpliendo las regulaciones locales respecto al transporte de agentes biológicos.
PROCEDIMIENTO DE ENSAYO
1) Llevar las muestras y tampón y dispositivos a temperatura ambiente si están refrigerados o congelados. Colocar el dispositivo en un lugar limpio de superficie plana.
2)
Para sangre entera
Dispensar 1 gota de sangre total (alrededor de 40-50 uL) en el pocillo de muestra. A continuación, añadir 2 gotas (aproximadamente 80 uL) del tampón inmediatamente.
Para suero o plasma
Dispensar 1 gota (alrededor del 40 uL) de la muestra en el pocillo de muestra, asegurándose de que no hay burbujas de aire. A continuación añadir 1 gota (aproximadamente 40 uL) del diluyente de la muestra inmediatamente.
3) Los resultados pueden ser leídos en 15 minutos. Los resultados positivos pueden ser visibles a partir de 1 minuto. No lea el resultado después de 30 minutos.
INTERPRETACIÓN DEL RESULTADO
- RESULTADO POSITIVO:
Una banda roja aparece en la región de control (C) y otra banda de color aparece en la región de la banda T.
- RESULTADO NEGATIVO: Una banda de color aparece 1n la región de control (C). No se observa banda en la región de la banda de prueba (T).
- RESULTADO NO VÁLIDO:La banda de control no aparece en el período de 15 minutos. Por favor, revise el procedimiento y repetir con una nueva prueba. Si el problema persiste, deje de utilizar el kit y contacte con su distribuidor local.
* NOTA: Las muestras con resultados positivos deben ser confirmadas con un método alternativo y además deben existir signos clínicos y/o alteraciones hematobioquímicas. Los animales con signos clínicos y resultado negativo deben ser igualmente confirmados. El test de confirmación se realiza gratuitamente en Laboratorio Dr. Barba.
CONTROL DE CALIDAD
Existen controles de calidad a su disposición, disponibles bajo pedido.
EFICACIA DEL TEST
La sensibilidad relativa al test ELISA es del 91,2% y la especificidad del 99,5%, siendo la concordancia del 98,3%.
LIMITACIONES DEL TEST
1) El procedimiento de ensayo y la interpretación de resultados de pruebas deben ser respetados de forma estricta. Si no sigue el procedimiento puede dar resultados inexactos.
2) El test Leishmania Ab Prueba Rápida se limita a la detección cualitativa de anticuerpos para
L. donovani en sangre, suero o plasma. La intensidad de la banda de ensayo no tiene una correlación lineal con el título de anticuerpos en la muestra.
3) Un resultado negativo para un sujeto individual Indica ausencia de anticuerpos anti-L. donavani
por encima de la línea de corte. Sin embargo, un resultado negativo no excluye la posibilidad de exposición a L. donovani.
4) Se puede producir un resultado negativo si la cantidad de los anticuerpos presentes contra L. donovani está por debajo de los límites de detección del ensayo, o los anticuerpos no están presentes durante la etapa de la enfermedad en que se recoge la muestra.
5) Algunas muestras que contienen títulos altos de anticuerpos heterófilos o factor reumatoide pueden afectar a los resultados esperados.
6) Los resultados obtenidos con esta prueba sólo deben interpretarse en conjunción con otros procedimientos diagnósticos y hallazgos clínicos.
REFERENCIAS
1. WHO. Control of the Leishmaniasis. World Health Organization. Technical Report Series 1990. No. 793.
2. Rosenthal E, Marty P. Visceral leishmaniasis. Rev Prat 2004;54(20):2211»6.
3. Molina R, Gradoni L, Alvar ]. HIV and the transmission of Leishmania. Ann Trop Med Parasitol. 2003 ;97 Suppl 1:29~45.
4. Allain DS, Kagan IG. A direct agglutination test for leishmaniasis. Am j Trop Med Hyg. 1975 ;24(2):232-6.
5. Badaro R, Reed 56, Carvalho EM. Immunofluorescent antibody test in American visceral leishmaniasis: sensitivity and specificity of different morphological Am I Trop Med Hyg. 1983;32(3):480-4.
6. Maalej IA, Chenik M, Louzir H, Ben Salah A, et, al. Comparative evaluation of ELISAs based on ten recombinant or purified Leishmania antigens for the serodiagnosis of Mediterranean visceral leishmaniasis. Am I Trop Med Hyg. 2003 68(3):312-20.
7. Burns [M It, Shreffler WG, Benson DR, Ghalib HW, Badaro R, Reed SG. Molecular characterization of a kinesin-related antigen of Leishmania chagasi that detects specific antibody in African and American visceral leishmaniasis. Proc Natl Acad Sci U S A. 1993 Jan 15;90(2):775-9.